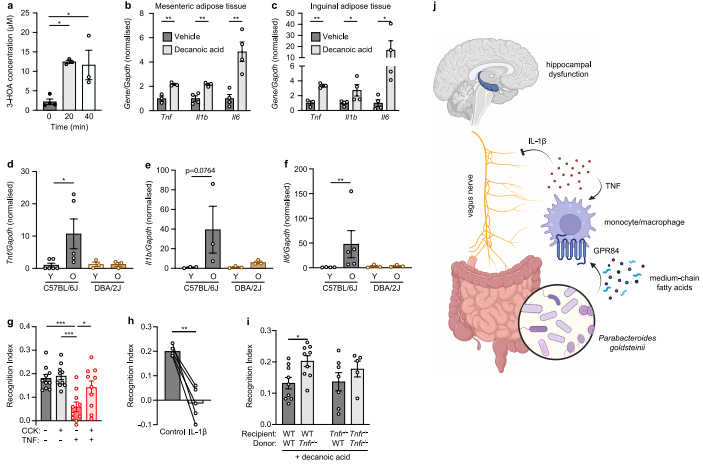
年龄相关认知衰退严重影响老年人生活质量,海马体神经元记忆编码能力随年龄下降的机制尚未完全明确,而肠道菌群作为可调节的外周信号,其与脑功能的具体调控通路一直是研究盲区。近日,斯坦福大学Christoph AThaiss团队在国际顶刊《Nature》发表重磅研究,首次揭示肠道内感受功能障碍是驱动认知衰退的核心机制,发现老年小鼠肠道中富集的Parabacteroides goldsteinii可通过产生中链脂肪酸激活GPR84炎症通路,抑制迷走神经-海马体信号传导,且噬菌体靶向清除、GPR84抑制等干预手段可逆转该表型,为对抗年龄相关认知衰退提供了全新方向。 组学检测技术:16S微生物多样性、宏基因组、原核转录组、蛋白组、代谢组、转录组、单细胞转录组 肠道菌群的年龄相关改变是否为年龄相关认知衰退的关键驱动因素,且该效应是否可传递、可逆转?介导该效应的核心菌群、代谢物及关键分子靶点是什么?菌群信号如何通过肠-脑轴(神经-免疫机制)影响海马体功能,最终导致记忆障碍? 研究团队首先通过异体共居和粪菌移植实验发现,将老年小鼠的肠道菌群移植给年轻小鼠后,年轻小鼠出现显著记忆缺陷,这一现象在新物体识别、Barnes迷宫等多种行为学测试中得到验证。基于这一观察,研究者提出核心假设:肠道菌群的变化可能是年龄相关认知衰退的驱动因素,而非单纯的伴随现象。 为验证这一假设,研究人员对小鼠全生命周期的肠道菌群进行宏基因组学和蛋白质组学追踪,结合共居/FMT实验中菌群的可传播性,通过“年龄相关性+可传递性+认知相关性”的优先级评分,筛选出关键菌种Parabacteroides goldsteinii。通过单菌定植实验,证实P. goldsteinii单独即可诱导认知障碍,并导致海马体神经元激活受损。 在机制层面,研究者通过代谢组学分析发现P. goldsteinii培养上清中的中链脂肪酸(MCFAs)是效应分子。利用GPR84基因敲除小鼠和骨髓嵌合体模型,证实MCFAs通过激活外周髓系细胞表面的GPR84受体诱发局部炎症。进一步通过化学遗传学、神经元亚群特异性消融和在体钙成像技术,精确定位PHOX2B+TRPV1+迷走神经传入纤维是肠-脑信号传导的关键中继站,并发现IL-1β是直接作用于迷走神经元导致其功能障碍的效应分子。 在机制明确的基础上,研究进一步探索临床转化潜力。通过噬菌体靶向清除P. goldsteinii、GPR84拮抗剂PBI-4050阻断炎症信号、低剂量辣椒素或肠道激素(CCK/GLP-1)激活迷走神经等多种干预手段,均证实能够有效恢复老年小鼠的认知功能。基于这些发现,研究提出“内感受功能障碍”驱动大脑衰老的新理论,并首创“内感受模拟剂”概念,为抗认知衰退药物研发提供了全新策略。 研究思路小结:本研究从临床现象出发,依次完成“因果确立—关键菌筛选—分子机制解析—神经环路定位—干预验证”的逐层深入探究,系统揭示了一条从肠道菌群,经代谢物-免疫-神经信号级联放大,最终影响海马体功能的肠-脑轴调控通路。 菌群对认知衰退的影响及认知衰退的微生物驱动因子肠道菌群的年龄相关改变是驱动年龄相关认知衰退的关键因素,且该效应具有可传递性和可逆性。通过年轻与老年小鼠共居实验,年轻小鼠菌群向老年样转变,同时出现短期记忆(新物体识别实验)和空间学习能力(Barnes迷宫)下降,且该表型在雌雄小鼠及不同品系小鼠中均稳定存在。 粪便微生物粪菌移植(FMT)实验证实,将老年小鼠的菌群移植给无菌小鼠,可直接诱导受体小鼠出现认知障碍;反之,年轻小鼠的菌群未显示该效应。 无菌小鼠与老年无菌小鼠共居后未出现认知下降,排除了社会互动等非菌群因素的干扰;而抗生素消融菌群可逆转共居诱导的年轻小鼠认知缺陷,且老年小鼠经抗生素处理后认知功能也得到改善,进一步验证菌群是认知衰退的核心驱动者。 Parabacteroides goldsteinii是介导年龄相关认知衰退的关键致病菌,其丰度随年龄升高且可通过菌群传递。 对小鼠全生命周期菌群的宏基因组、16S rDNA测序及粪便蛋白质组分析发现,1133种细菌的相对丰度随年龄变化,其中Parabacteroides goldsteinii是排名第一的候选致病菌。 功能验证显示,将Parabacteroides goldsteinii单菌定植于无菌小鼠或抗生素消融后的小鼠体内,可独立诱导认知障碍;而自然携带高丰度该菌的年轻小鼠,其记忆功能显著低于低丰度小鼠。 其他年龄相关菌群(如属、毛螺菌科)或非年龄相关菌群(如嗜酸乳杆菌),均未表现出类似的认知调控效应,证实是认知衰退的特异性微生物驱动因子。 图1 微生物组对年龄相关性认知功能衰退的影响









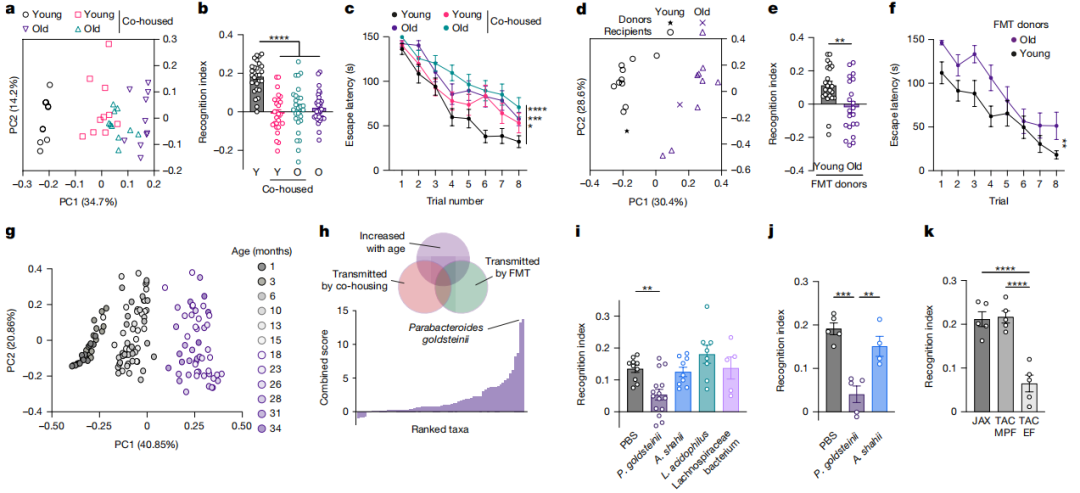

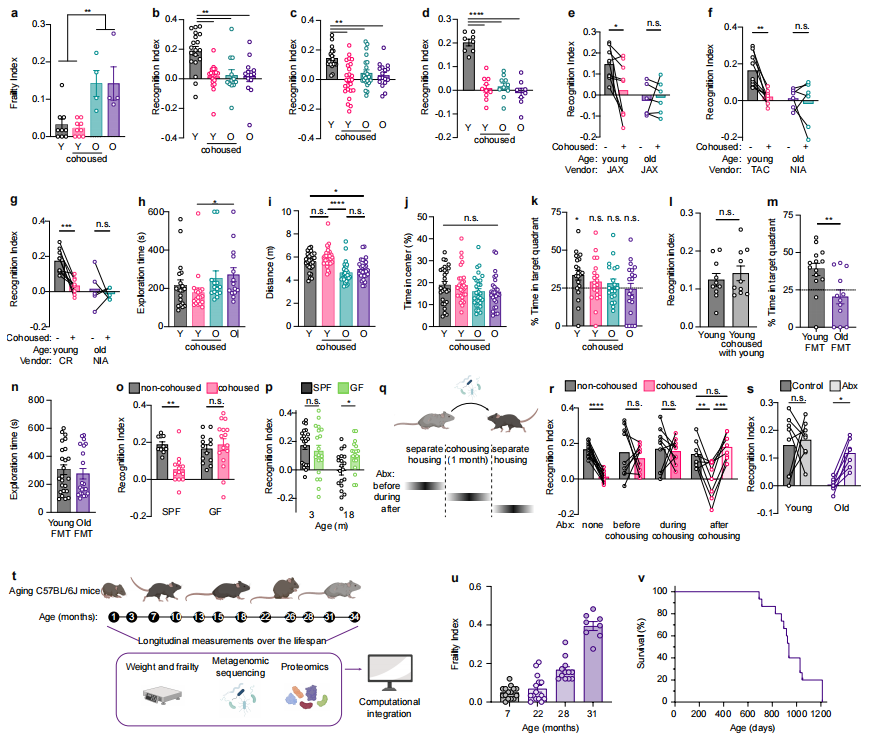

图2 衰老微生物组损害认知功能
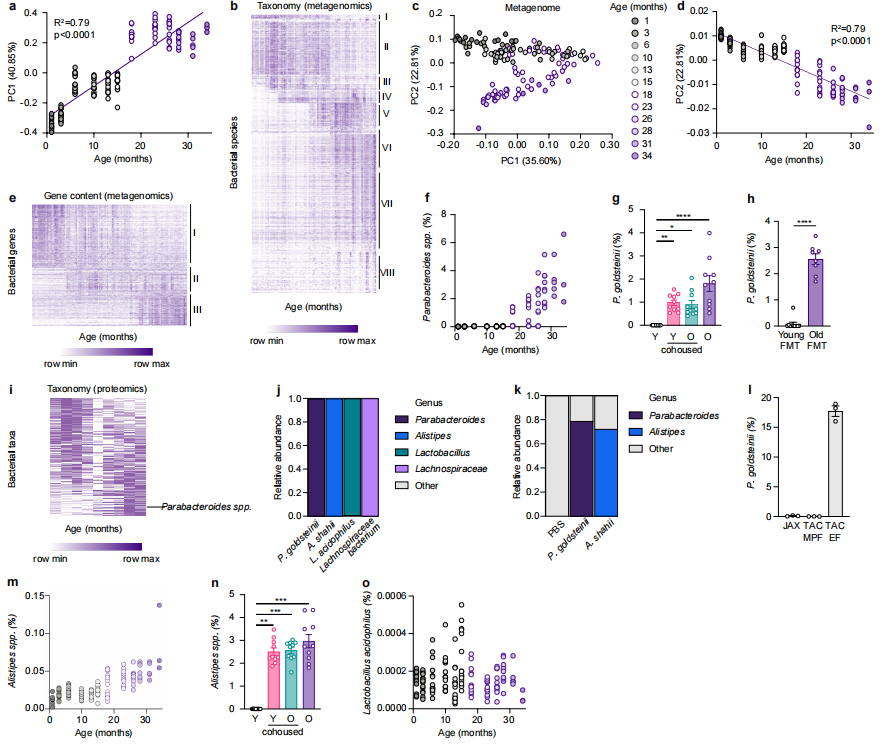

图3 生命周期中的微生物组变化
菌群老化引发的大脑响应 菌群老化通过削弱关键脑区的神经元激活能力(尤其是海马体记忆编码相关激活)驱动认知衰退,且不依赖海马体自身结构改变。 通过对共居获得老年样菌群、移植老年小鼠菌群或定植Parabacteroides goldsteinii的小鼠海马体进行转录组检测,发现海马体CA1、CA3、齿状回区域的即时早期基因(Fos、Egr1等)表达下调,FOS⁺阳性神经元数量减少,神经元对新异刺激的激活能力显著受损。 进一步实验证实,菌群老化的影响并非局限于海马体,孤束核、躯体感觉皮层、内嗅皮层等参与感觉处理的脑区,均出现神经元激活减弱的响应。 此外,实验未检测到海马体神经发生减少、星形胶质细胞活化或树突棘可塑性异常,排除了海马体自身结构改变的影响;且抗生素消融菌群或靶向干预致病菌可逆转神经元激活缺陷,验证该响应由菌群老化特异性驱动。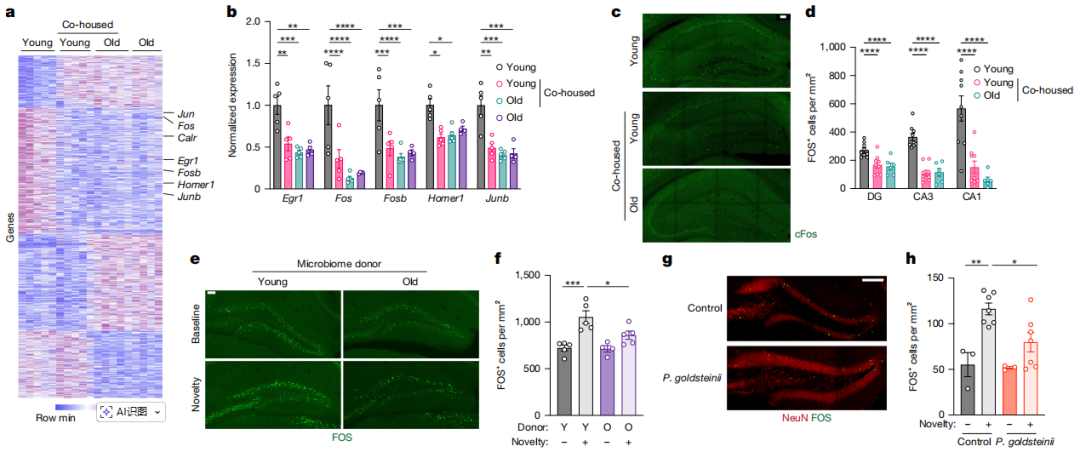

图4 大脑对微生物组衰老的反应
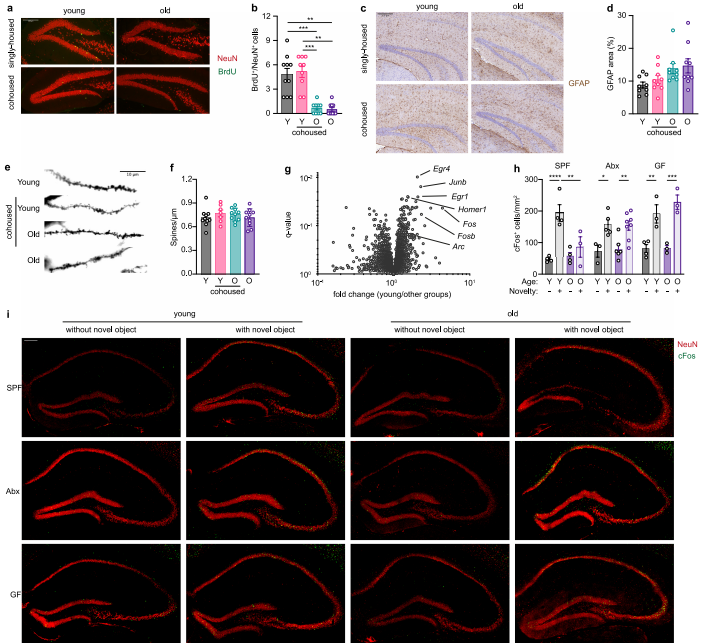

图5 微生物组对脑衰老的影响
内感受功能障碍与记忆丧失 内感受功能障碍(肠道-大脑感觉信号传导受损)是菌群老化诱导记忆丧失的核心机制,且依赖迷走神经(尤其是PHOX2B⁺TRPV1⁺亚型)功能抑制。 通过对Trpv1⁻/⁻基因敲除小鼠或化学遗传学沉默TRPV1⁺神经元的实验发现,缺失TRPV1⁺感觉神经元会导致小鼠海马体激活缺陷,模拟老年小鼠的记忆障碍表型;反之,化学遗传学激活TRPV1⁺神经元或给予TRPV1激动剂辣椒素,可恢复共居小鼠、老年小鼠的海马体功能及记忆能力。 进一步利用Phox2b特异性标记(迷走神经而非脊髓传入神经)实验证实,沉默PHOX2B⁺迷走神经可重现记忆缺陷,而靶向脊髓传入神经无此效应;双光子钙成像显示,携带老年样菌群的小鼠迷走神经对肠道营养刺激的响应性神经元数量减少、激活强度降低,直接验证迷走神经传导功能受损。 此外,补充肠-脑轴激活肽(CCK、GLP-1)可通过激活迷走神经逆转记忆丧失,且该效应依赖TRPV1⁺神经元存在,证实内感受信号传递障碍是连接菌群老化与记忆丧失的关键环节。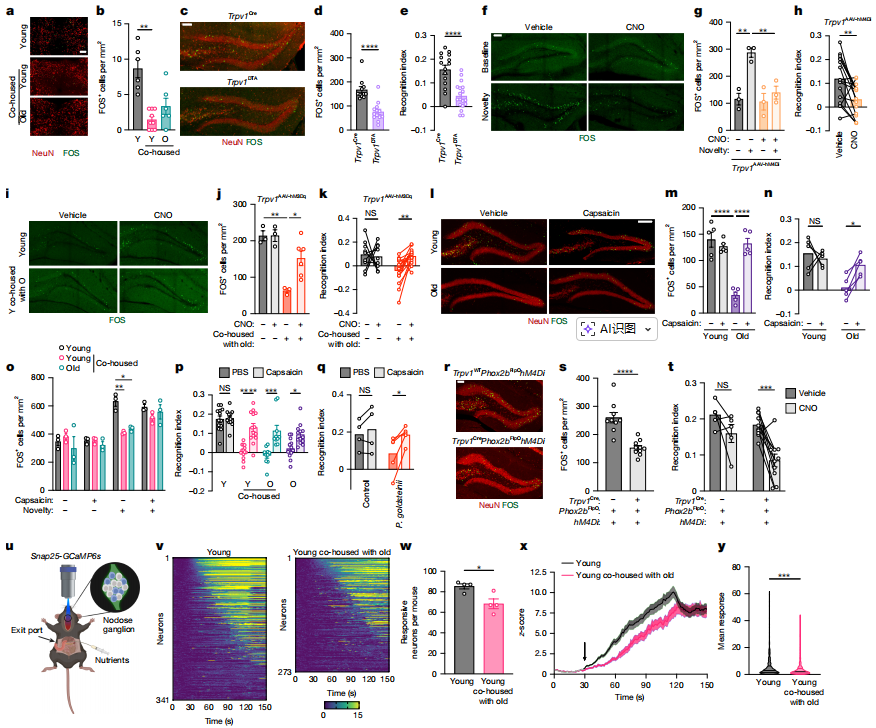

图6 肠道-脑信号传导受损导致认知功能障碍
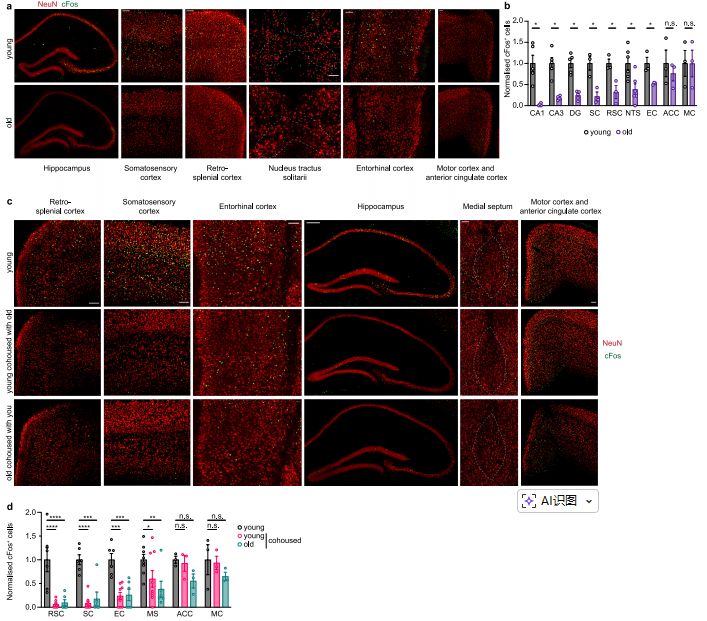

图7 衰老微生物组损害神经元对新奇刺激的反应
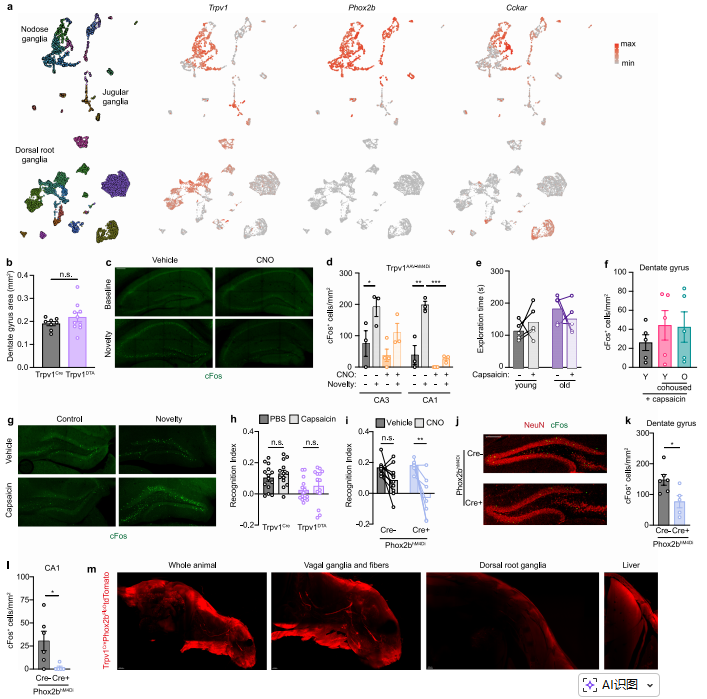

图8 TRPV1阳性神经元调控认知功能
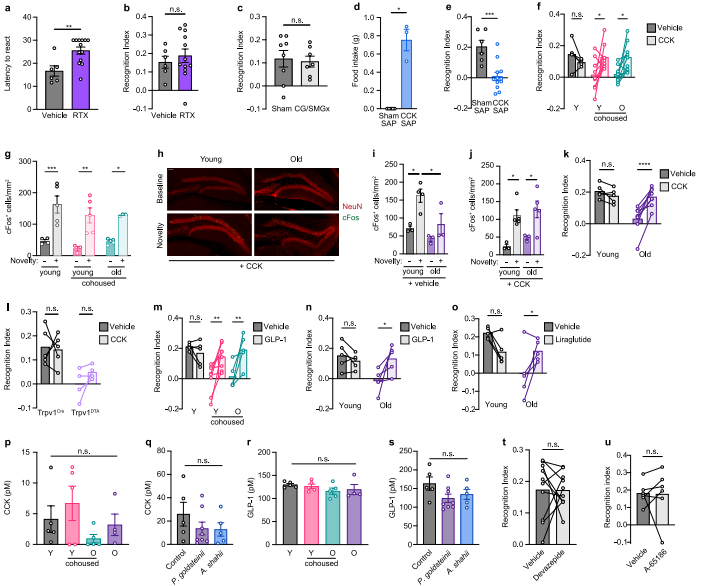

图9 传入感觉输入调节认知
肠道代谢物与认知衰退 中链脂肪酸(MCFA,如3-羟基辛酸、癸酸、十二酸)是介导菌群老化诱导认知衰退的关键效应代谢物,其积累可模拟菌群老化引发的认知损伤效应。 通过对关键致病菌Parabacteroides goldsteinii培养上清的分离筛选及非靶向代谢组学分析,发现该菌分泌的小分子代谢物(<3 kDa)可独立诱导认知障碍,进一步鉴定出MCFA为核心效应分子。 靶向代谢组学验证显示,小鼠肠道内MCFA水平随年龄增长而升高,且可通过共居或粪便微生物移植(FMT)从老年小鼠传递给年轻小鼠;口服补充MCFA可重现海马体神经元激活缺陷及记忆障碍,其效应与定植P. goldsteinii或移植老年菌群一致。 此外,靶向抑制MCFA产生(如噬菌体φPDS1处理)可降低肠道MCFA水平并改善老年小鼠认知功能,证实MCFA是菌群与认知衰退之间的关键代谢桥梁。 图10 MCFA通过GPR84介导的信号传导驱动记忆丧失 图11 中链脂肪酸(MCFAs)在衰老过程中以微生物组依赖性方式增加,并可通过噬菌体治疗减少 肠道炎症与迷走神经功能障碍 MCFA通过激活外周髓系细胞GPR84受体诱发局部炎症,进而抑制迷走神经功能,最终阻断肠-脑认知信号传导。 通过Gpr84⁻/⁻基因敲除小鼠实验证实,MCFA的认知损伤效应依赖GPR84受体;单细胞转录组测序及功能验证显示,GPR84仅表达于外周髓系细胞(巨噬细胞、单核细胞、中性粒细胞),耗竭外周髓系细胞可逆转MCFA诱导的认知缺陷。 机制上,MCFA激活髓系细胞GPR84后,会促进TNF、IL-1β等促炎因子释放;双光子钙成像及神经功能检测显示,这些炎症因子会直接削弱迷走神经对肠道刺激的响应能力(响应神经元数量减少、激活强度降低)。 进一步实验证实,中和TNF/IL-1β炎症因子或抑制GPR84活性,可恢复迷走神经传导功能及海马体神经元激活,逆转认知衰退,证实肠道局部炎症是连接MCFA与迷走神经功能障碍的关键环节。 图12 外周髓系细胞上的GPR84信号传导通过炎症激活驱动认知功能下降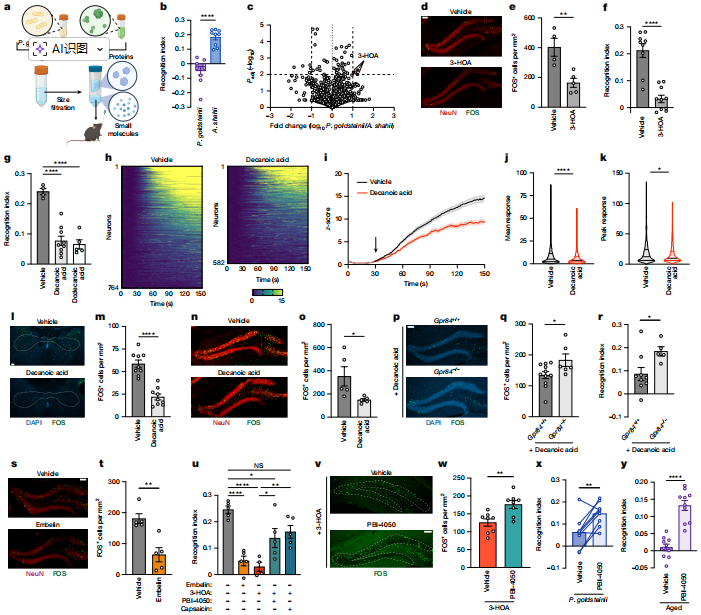

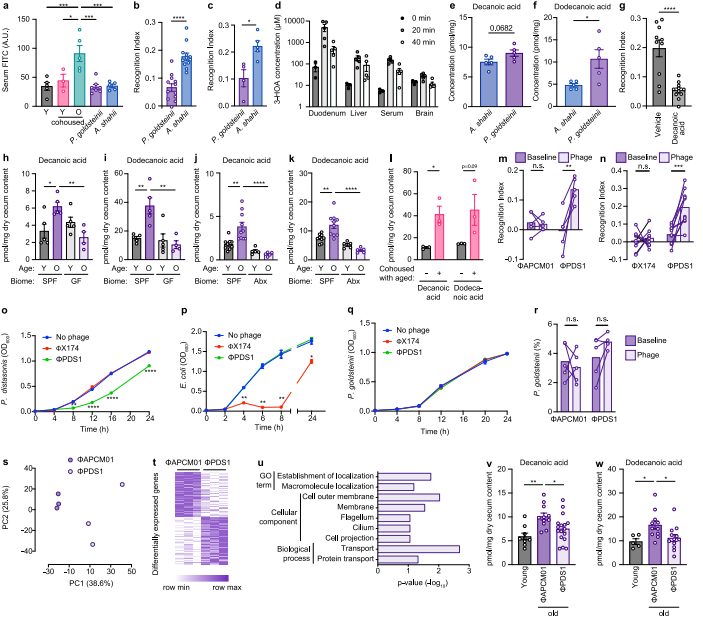

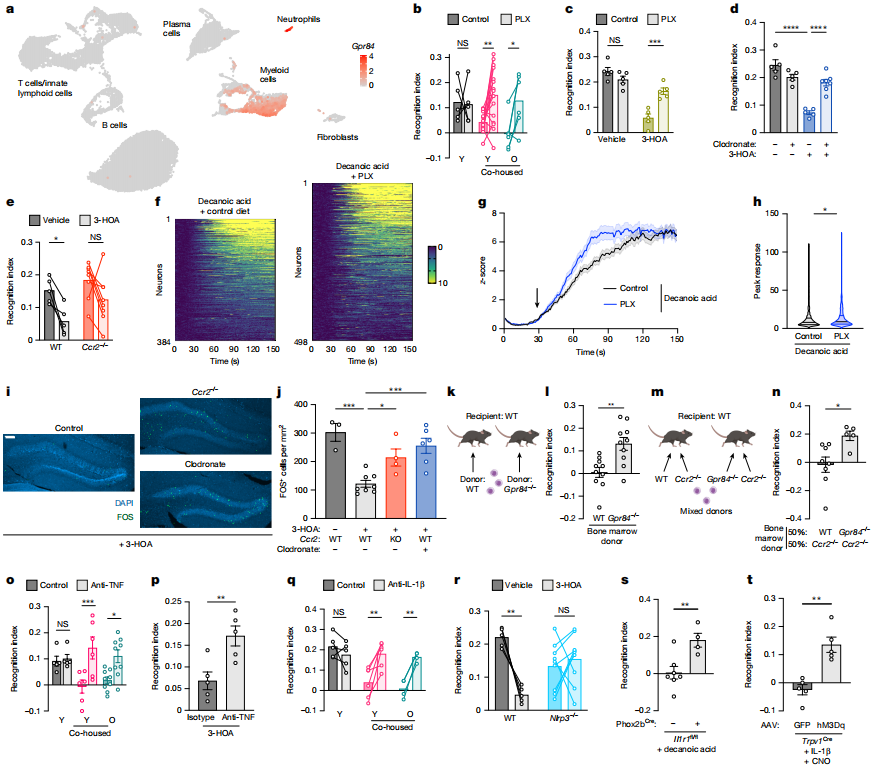

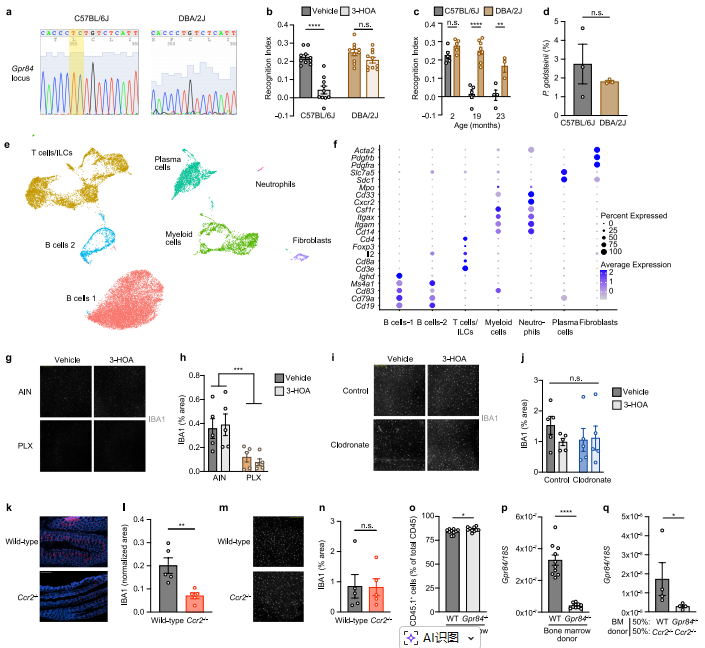

图13 GPR84与髓系细胞的影响
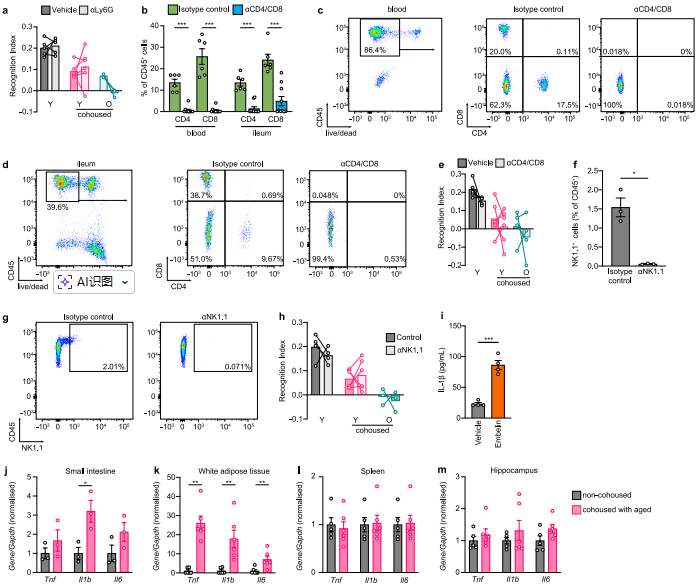

图14 老化微生物组诱导的外周炎症分析
图15 GPR84信号传导驱动外周炎症 该研究揭示了肠道菌群调控年龄相关认知衰退的完整机制,整合宏基因组、16S rDNA测序、粪便蛋白质组、代谢组学及转录组、单细胞转录组等多组学技术,锁定核心致病菌Parabacteroides goldsteinii及其分泌的中链脂肪酸(MCFA)。MCFA通过激活外周髓系细胞GPR84受体诱发局部炎症,抑制PHOX2B⁺TRPV1⁺迷走神经功能,导致海马体等脑区即时早期基因表达下调、神经元激活受损,最终引发记忆衰退。抗生素消融菌群、噬菌体靶向致病菌、GPR84抑制或迷走神经激活等干预手段可逆转该表型。研究以多组学为核心技术支撑,明确了肠-脑轴内感受功能障碍的关键作用,为认知衰退提供了全新干预方向。 机制新:首次提出肠道内感受功能障碍是年龄相关认知衰退的核心驱动机制,明确了肠-脑轴感知异常在脑老化中的关键作用。 靶点新:鉴定出Parabacteroides goldsteinii为调控认知衰退的关键肠道菌,及其产生的中链脂肪酸(MCFA)为核心效应代谢物。锁定菌群-代谢物层面的精准干预靶点。 通路新:阐明“菌群-MCFA-外周髓系细胞GPR84-炎症因子-迷走神经-海马体”的完整调控链,首次证实外周局部炎症(非全身/中枢炎症)可通过抑制迷走神经活性削弱海马体神经元功能,明确GPR84是菌群信号向神经系统传递的核心枢纽。 干预新:验证了噬菌体靶向致病菌、GPR84抑制剂、迷走神经激活剂等多类靶向该通路的干预手段,均能逆转衰老相关认知衰退,为临床转化提供了多元化的全新策略。 参考文献 https://doi.org/10.1038/s41586-026-10191-6